
约40%-50%的乳腺癌(breast cancer,BC)患者处于HER2低水平表达状态,但以往经典的抗HER2靶向药物(wù)在HER2低表达领域“表现欠佳”。 抗體(tǐ)-药物(wù)偶联物(wù)(Antibody-drug Conjugate, ADC)兼具了传统化疗的强大杀伤力和抗體(tǐ)药物(wù)的肿瘤靶向性,近20余年来在BC领域发展迅速。

日前,第25届全國(guó)临床肿瘤學(xué)大会暨2022年CSCO乳腺癌专家委员会内分(fēn)泌专场圆满落幕。会上王晓稼教授进行了题為(wèi)《抗體(tǐ)-药物(wù)偶联物(wù)(ADC)在HER2低表达领域治疗机会》的报告,為(wèi)各位學(xué)者总结了当前ADC药物(wù)的迅速发展对临床治疗产生的巨大影响。医學(xué)界特為(wèi)此内容作出报道。
ADC药物(wù)的起源与发展
王晓稼教授介绍到,ADC的概念最早在100多(duō)年前提出,后直至2000年,首个ADC药物(wù)曲妥珠单抗获批上市。ADC药物(wù)的问世,改变了近20年来实體(tǐ)瘤领域的临床实践和疗效。
新(xīn)一代靶向ADC药物(wù)的“强旁观者效应”、“直接杀伤HER2 1+和2+细胞”以及“稳定精准的靶性递送”三重特点,使其具有(yǒu)强效的抗肿瘤作用(yòng)。目前ADC是抗肿瘤药物(wù)研发非常重要的领域,相继已有(yǒu)多(duō)款新(xīn)药研发上市,如國(guó)内的抗HER2治疗药物(wù)RC48(维迪西妥单抗)、A166,抗Trop2治疗药物(wù)BAT8003等,國(guó)外一鸣惊人的靶向HER2治疗药物(wù)T-DXd,靶向Trop-2的ADC药物(wù)戈沙妥珠单抗(Sacituzumab govitecan,SG)等。
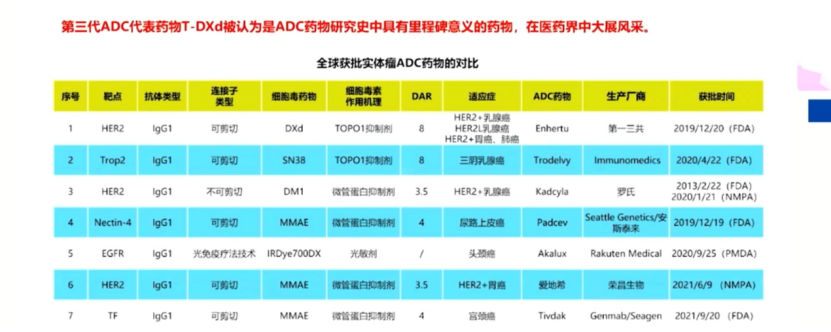
【全球获批实體(tǐ)瘤ADC药物(wù)对比-截图来自王晓稼教授报告】
既往多(duō)项研究在HER2低表达BC领域频频失利,新(xīn)型ADC药物(wù)的出现在多(duō)个癌种领域展现了巨大的临床价值,王晓稼教授特别介绍了DESTINY-Breast系列试验在HER2低表达BC领域迄今取得的优异成果。
• DESTINY-Breast 01(DB-01): T-DXd初露锋芒
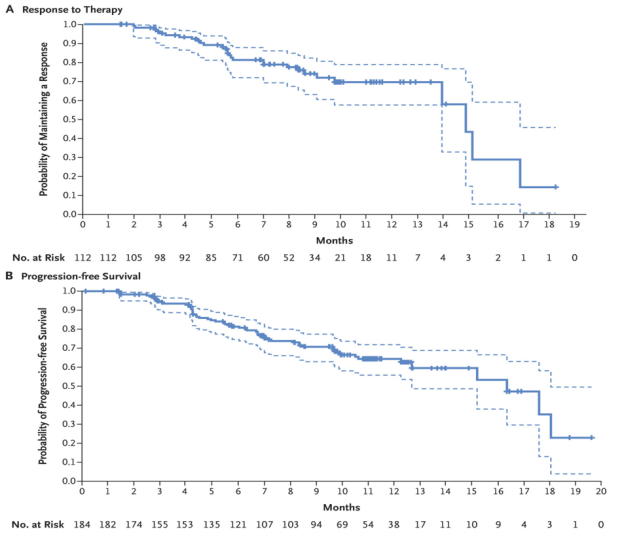
DB-01研究中纳入HER2+不可(kě)切除或转移性BC且既往接受过T-DM1治疗的成年患者,研究结果显示,在既往中位治疗為(wèi)6線(xiàn),184例接受推荐剂量(5.4mg/kg)治疗的患者中,缓解率(ORR)為(wèi)60.9%,中位无进展生存期(PFS)达16.4个月,中位持续缓解时间(DOR)达14.8个月。
• DESTINY-Breast 03(DB-03):树立晚期BC治疗新(xīn)标准
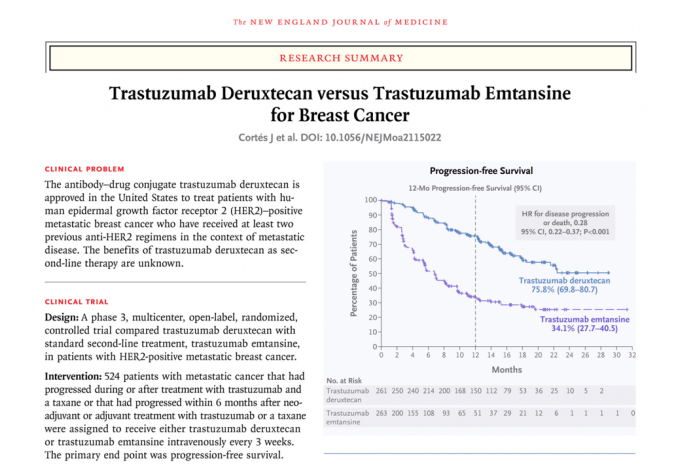
DB-03研究中纳入HER2+ 不可(kě)切除或转移性BC患者,按1:1比例随机分(fēn)配接受T-DXd或T-DM1治疗,研究结果显示T-DXd组的ORR较T-DM1组高出一倍多(duō)(79.7% vs 34.2%),较T-DM1组的PFS也有(yǒu)显著改善(NR vs 6.8个月;HR 0.28; 95%CI 0.22~0.37;P<0.001)。T-DXd由此获得NCCN、ASCO、ESMO等权威指南推荐。
• DESTINY-Breast 04(DB-04):打破HER2阴阳二分(fēn)格局
DB-04研究中纳入既往接受过一線(xiàn)或二線(xiàn)化疗的HER2低表达(定义為(wèi)IHC 1+/IHC 2+且ISH阴性)的不可(kě)切除或转移性BC患者,以2:1的比例随机分(fēn)配接受T-DXd治疗或医生选择的化疗(TPC,仅限于卡培他(tā)滨、艾日布林、吉西他(tā)滨、紫杉醇和白蛋白紫杉醇)。研究结果显示,在HR+患者中,T-DXd组中位PFS為(wèi)10.1个月(95%CI 9.5-11.5),而TPC组為(wèi)5.4个月(95%CI 4.4-7.1)(HR 0.51;95%CI 0.40-0.64;P<0.001),OS分(fēn)别為(wèi)23.9个月vs 17.5个月(HR 0.64;95%CI 0.48-0.86;P=0.003)。
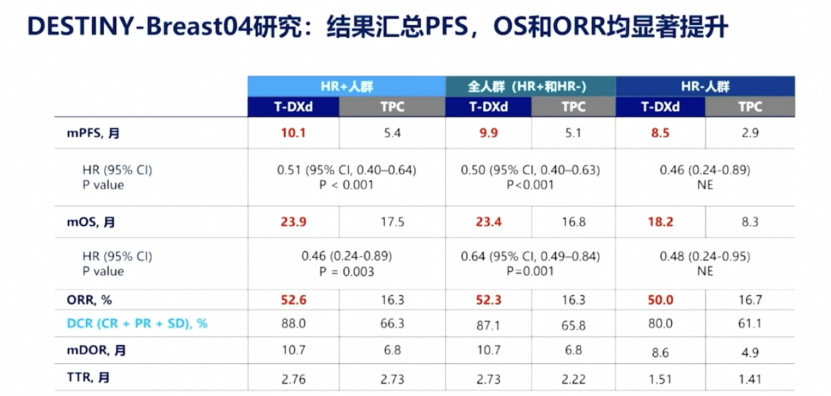
DB-04研究的震撼发布推动了2022年NCCN和ASCO指南的快速更新(xīn):针对HER2低表达的不可(kě)切除或转移性BC患者,既往在转移性疾病阶段接受过至少一次化疗,如激素受體(tǐ)阳性(HR+)则為(wèi)内分(fēn)泌难治性,应给予T-DXd治疗。T-DXd的出现标志(zhì)着HER2低表达BC患者的治疗格局将被改写。
此外,2022年8月5日,美國(guó)FDA基于DB-04批准T-DXd用(yòng)于无法切除或转移的HER2低表达BC患者,这是临床上首个针对HER2低表达患者的治疗药物(wù),為(wèi)乳腺癌患者的生存改善提供了更多(duō)可(kě)能(néng),对乳腺癌治疗领域意义非凡。
HER2低表达晚期乳腺癌的治疗变革
HER2低表达在CSCO-BC 2022版定义為(wèi)IHC 1+/IHC 2+且ISH阴性。T-DXd出现前的较長(cháng)一段时间里,HER2低表达患者处于一种“无药可(kě)用(yòng)”的状态,大多(duō)被归為(wèi)HER2阴性亚型中进行内分(fēn)泌治疗或化疗。
王晓稼教授提到,既往多(duō)项研究表明,传统的靶向治疗(如曲妥珠单抗、帕妥珠单抗、T-DM1等)在HER2低表达领域效果不理(lǐ)想,且HER2表达水平和预后之间没有(yǒu)明显的相关性,即HER2低表达对临床预后的预测能(néng)力一般,尚不能(néng)作為(wèi)分(fēn)子分(fēn)型的重要参数。
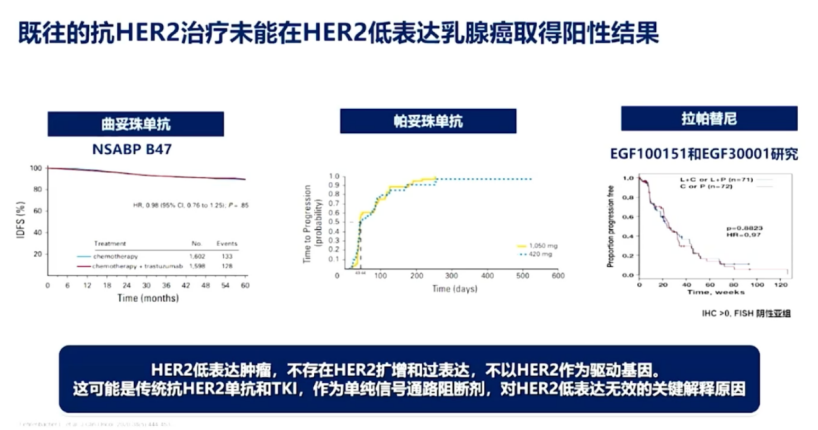
王晓稼教授谈到, HER2低表达的患者長(cháng)期以来对安全、有(yǒu)效的治疗有(yǒu)着大量未被满足的需求,随着越来越多(duō)新(xīn)型ADC药物(wù)的开发研制,我们有(yǒu)理(lǐ)由相信在不遠(yuǎn)的未来,HER2低表达的BC患者也将从精准的靶向治疗中获益。
T-DXd作為(wèi)新(xīn)一代ADC药物(wù)的佼佼者,除了BC领域,在其他(tā)实體(tǐ)瘤HER2低表达领域的研究也收获颇丰。如2020年ESMO年会报道了DESTINY- Gastric01研究中HER2低表达探索性队列的相关结果。
• DESTINY- Gastric01:展现T-DXd治疗HER2低表达胃癌的初步疗效
DESTINY- Gastric01是一项随机、开放标签、多(duō)中心、II期临床试验,主要目的在于对比T-DXd和化疗两种方案治疗HER2阳性转移性胃癌的疗效,同时在探索性队列中探讨了T-DXd对HER2低表达人群的临床获益情况。
研究结果表明,在探索队列中,队列1(HER2 IHC2+/ISH-)患者19例,队列2(HER2 IHC1+)患者21例。队列1的ORR达36.8%,中位DOR 7.6个月,中位OS 7.8个月,中位PFS 4.4个月;队列2 ORR达19%,中位DOR 12.5个月,中位OS 8.5个月,中位PFS 2.8个月。显示出T-DXd在HER2低表达的晚期胃癌或胃食管交界处(GEJ)癌患者中,具有(yǒu)的良好抗肿瘤效果。
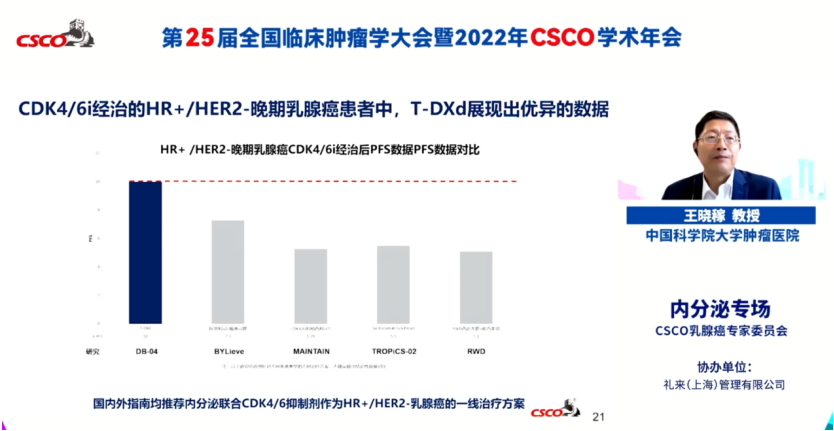
王晓稼教授补充道,目前CDK4/6i治疗失败的领域里I级治疗仍是空白的推荐,T-DXd用(yòng)于CDK4/6经治的HR+/HER2-晚期BC患者中表现优异,有(yǒu)望在明年写入指南,填补CDK4/6i经治分(fēn)层的空白。
除上述提到的ADC界“明星”药物(wù)T-DXd外,戈沙妥珠单抗(SG)在HER2低表达领域也占有(yǒu)一席之地。2022年ESMO大会对SG在TROPICS -02研究中HER2低表达亚组的分(fēn)析结果进行了报道。
SG是一款首创靶向TROP2的ADC药物(wù),TROP2在大约80%的BC中高表达,无论何种亚型。2022年6月7日SG被FDA批准用(yòng)于既往接受过2中系统治疗(至少1种治疗针对转移病变)的不可(kě)切除或转移的三阴性乳腺癌(TNBC)患者。
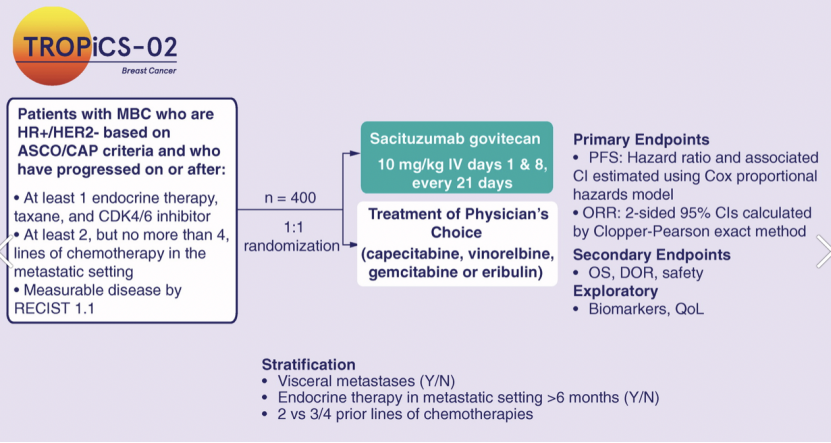
• TROPICS -02:走在TROP-2靶向ADC药物(wù)的前沿
TROPICS -02是一项全球多(duō)中心、随机、放标签、III期临床试验,主要目的旨在评估SG在接受过内分(fēn)泌治疗、CDK4/6抑制剂以及2~4線(xiàn)化疗的TNBC患者的临床疗效和安全性。
研究结果显示,在HER2低表达亚组,SG组的中位PFS优于TPC组(6.4 个月vs 4.2个月;HR 0.58;95%CI 0.42-0.79;P<0.001),与意向治疗人群(ITT)一致;OS分(fēn)别為(wèi)26% vs 12%(OR 2.52;95%CI 1.33-4.78),临床获益率(CBR):38%比19%(OR 2.50; 95%CI 1.46-4.30),中位缓解持续时间(DOR)為(wèi)7.4 个月vs 4.1个月。
此该研究结果表明,SG不但可(kě)以改善TNBC患者的临床结局,而且在HER2低表达人群中具有(yǒu)一致获益。即SG的疗效不受HER2表达状态(HER2-Low或HR +/HER 2 IHC0)的影响。但需注意的是,ESMO大会上也随即也有(yǒu)专家对此结论提出异议,认為(wèi)关于SG在HER2低表达人群中的获益情况尚待进一步研究证实。
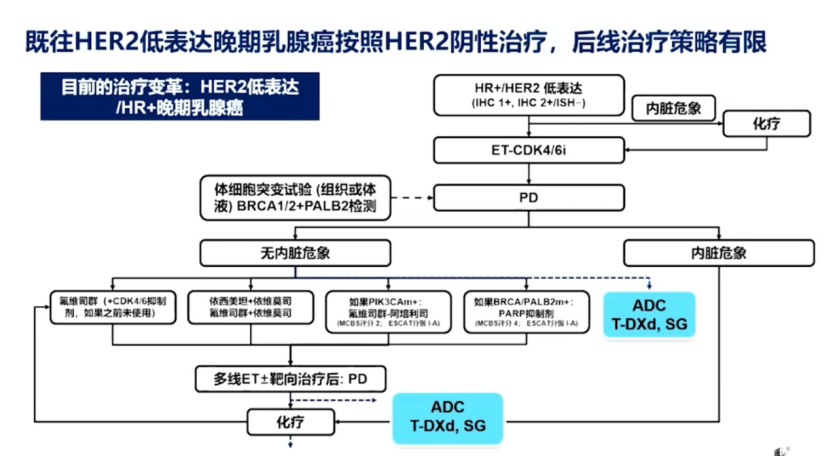
王晓稼教授表示,随着ADC药物(wù)的兴起,HER低表达/HR+晚期BC不再处于一种束手无策的局面,尽管当前國(guó)内药物(wù)可(kě)及性不如人意,但相信未来一定前景广阔。
ADC药物(wù)在HER2低表达乳腺癌中的未来探索
王晓稼教授强调,ADC药物(wù)在HER2低表达领域的潜力巨大,但现今仍面临诸多(duō)挑战。如HER2低表达的下限尚不明确,且HER2表达极具异质性,其状态也可(kě)能(néng)随着治疗而发生改变,如何准确识别HER2低表达人群对于临床研究及实践的开展至关重要。随后介绍了DESTINY-Breast 06和DESTINY-Breast 08两项极具前景的研究。
• DESTINY-Breast 06(DB-06):继续进军,未来可(kě)期
DB-06研究是一项聚焦于HER2低表达BC的III期临床试验,在DB-04基础上更进一步。研究纳入HER2低表达和超低表达(0<ihc<1+)的不可(kě)切除或转移性bc患者,随机接受t-dxd或tpc一線(xiàn)化疗。主要终点為(wèi)独立评估的pfs,次要终点有(yǒu)os、orr、dor等。< p="">

该研究将目标人群拓展至HER2超低表达人群,其成果将有(yǒu)助于识别T-DXd的适用(yòng)范围,或将推进T-DXd的治疗線(xiàn)序。
• DESTINY-Breast 08(DB-08):探索研究T-DXd联合治疗HER2低表达BC
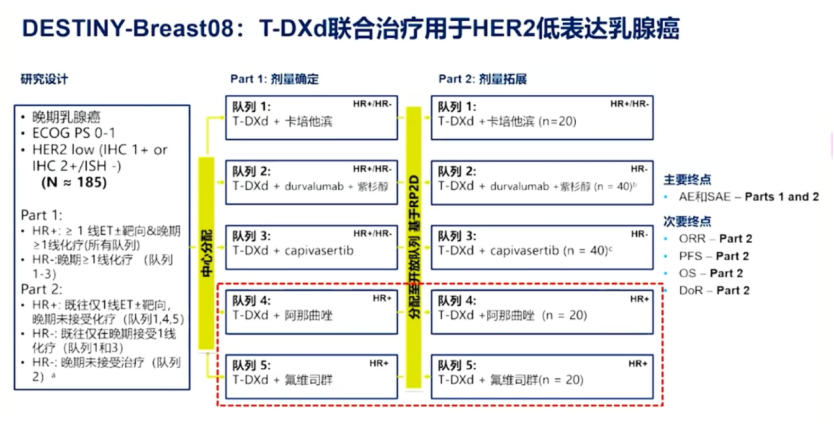
DB-08研究分(fēn)為(wèi)T-DXd+卡培他(tā)滨、T-DXd+durvalumab+紫杉醇、T-DXd+capivasertib、T-DXd+阿那曲唑、T-DXd+氟维司群共5个模块,旨在探索性研究T-DXd与其他(tā)抗癌药物(wù)联合使用(yòng)治疗转移性HER2低表达BC患者的安全性、耐受性、药代动力學(xué)及肿瘤活性。
王晓稼教授在演讲的最后表示,ADC药物(wù)治疗HER2低表达BC仍处于探索当中,T-DXd的出现对我们的传统治疗产生了巨大影响。除了T-DXd外,还有(yǒu)RC-48、SYD985、MRG002等ADC药物(wù)都进入到了积极的临床试验阶段,非常期待这样的研究能(néng)為(wèi)临床患者带来福音,挑战现有(yǒu)的标准治疗方案,进一步改变临床实践!
上一篇::乳腺癌精准诊疗病理(lǐ)學(xué)诊断要点暨全國(guó)临床肿瘤大会会议简要
下一篇::殷咏梅解读:HR+/HER2-晚期乳腺癌内分(fēn)泌分(fēn)层治疗